Сповільнюють нагрівання чаші й при безперервному перемішуванні скляною паличкою, випарюють розчин до консистенції сиропу
Отриманий розчин хлорного золота також служить для визначення проби в сплавах золота. Апробування сплавів золота розчином хлорного золота засноване на том. що при зіткненні сплавів з розчином хлорного золота вони розкладають його. При цьому хлор всту паст у сполуку з металом, а золото виділяється у вигляді осаду, який образуei на сплаві пляма
Металургійний сплав золота | і Гальванічний сплав, соогвет- | ||
і | | ствующии по кольору металу р-р- | | ||
і гическому й | |||
Сплав | Проба | Колір | | Сплав, Проба | |
і Золото -нікель | 850 1 Світле- | ! Золото-Нікель 825 - 875 1 | |
1. Золою-Срібло | 725 | сірий Зелене- | . Золото-Срібло | 725 - 776 | |
жовтий | ! | -j | ||
Золото-Мідь-Кадмій | 742 | Рожевий | і Золото-Мідь-Кадмій 700 - 800 і |
(7.5%Си, 8,3% Cd) | 1 і | ||
Золото-Мідь | 850 | Яркорозовий | Золото-Мідь 1 800 - 900 ). і |
Золото-Індій | 960 | Лимонножелтий | Золото-Індій | 950 - 970 ! |
Золото-Кобальтмедь (0.6%З, 0.2%Си) | 992 | Оранжевожелтий | Золото-Кобальтмедь | Г975 - 995 1. і. ! |
Сплав золото-мідь. Для гальванічного осадження сплаву золото-мідь застосовують ціаністий електроліт сліду ющего сполуки:.
Калій дицианоаурат [Kau(CN)
] (у перерахуванні на золото)...................3-4 г/л.
Калій ціаністий KCN..........................................................0,5-1. 5г/л.
Калій трицианокупрат K
Cu(CN)-,.............................................25-35 і >:.
Щільність струму..............................................................0.1-0.25 А/дм".
Кислотність........................................................................6.8-7.2рн.
Тем мература.............................................................................80С.
Анод - нержавіюча сталь марки 12Х18Н9 I.
Цей електроліт дозволяє одержати золотомедние покриття з найбільшою твердістю й кольором, близьким до кольору сплавів золота 585-й проби
Сплав золото-срібло. Для покриття сплаву золото-срібло застосовують ціаністий електроліт наступного сполуки:.
Калій дицианоаурат [Kau(CN)
] (у перерахуванні на золото).................8-10 г/л.
Калій ціаністий KCN.........................................................60-100 г/л.
Калій дицианоаргентат [Kag(CN)
] (у перерахуванні на срібло)............0.8-1,2.
Щільність струму...............................................................0.6-0.8 А/дм".
Кислотність........................................................................11-12 рН.
Температура.............................................................................22С.
Анод - нержавіюча сталь марки 12Х1 8Н9Т.
Сполука покриття залежить від умови осадження; низька температура електроліту й висока щільність струму підвищують зміст золота в покритті, і навпаки, підвищення температури електроліту, зниження щільності струму приводять до збільшення змісту срібла. Готування електроліту для осадження сплаву золото-срібло проводять розчиненням комплексних солей срібла й золота (мал. 4.4). Потім в отриманий розчин додають інші компоненти у вигляді розчинів
Сплав золото-мідь-кадмій. Осадження сплаву іолоіомедь-кадмий застосовують у ювелірній промисловості для одержання блискучих захисно-декоративних покриттів товщиною до 20 мкм.
Сполука електроліту для нанесення сплаву, що містить 70-75°» Аи. 12-24% Си й 6-8% Cd: Калій дицианоаурат [Kau(CN)
J (у перерахуванні на золото)..4,3-4.7 і л.
Калій ціаністий KCN...............................................15-20 г/л.
Калій трицианокупрат K
Cu(Cnh...............................45-55 і/л.
Калій тетрацианокадмат K
Cd(CN)
..............................1.0-1.2гл.
Кислота нитрилотриуксусная N(CH
COOH);,.......................5-7 г/л.
Аміак водний NH
OH (25%-ний).............................10-20 мол/л.
Плотност ь струму....................................................0,8-1,0 А/дм".
Кислотність........................................................10,0-10.5рн.
Температура...............................................................55-65°С
 |
Рис. 4.4 |
У якості анодів у цьому електроліті рекомендують застосовувати золото, платину, вугілля або нержавіючу сталь 12Х18Н10Т. При роботі з нерозчинними анодами кількість металу, виділюване на виробах, що покриваються, і уносимое ними при вивантаженні з ванни, компенсують шляхом періодичного або постійного додавання концентрованого розчину хлорного золо га.
Готування неціаністого електроліту. Для готування 1-го літра електроліту треба розчинити 2 і металевого золота в «царській горілці» або побрати 2,65 г хлорного золота
Розчинення золота в «царській горілці» (І часіь азотної кислоти, 3 частини соляної кислоти) проводять за схемою, описаної в п. 4.1.
Розчин солі золота, отриманий після полною розчинення золота в «царській горілці», нейтралізують за допомогою розчину вуглекислої) калію (поташ), доливаючи його до повного припинення виділення пухирців
Auci, Рис. 4.6.
Процес готування електроліту здійснюється в наступному порядку (мал. 4.7). Готовлять два розчини: перший - розчин железисто-синеродистого калію в 400 мол теплої дистильованої води й другий - розчин кальцинованої соди в 200 мол теплій дистильованої води
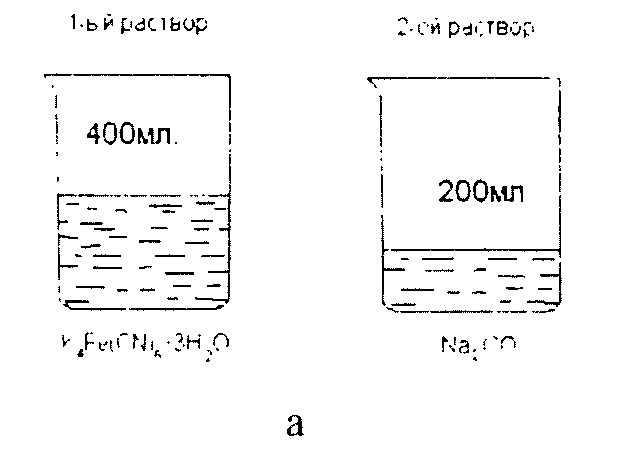

Потім обоє розчину вливають в одну ємність і кип`ятять .
У киплячий розчин повільно додають отриманий але схемі, описаної вище (4.1), розчин хлористого золота. При додаванні розчину хлористого золота електроліт каламутніє, потім ухвалює темно-коричневий колір. Отриманий у такий спосіб електроліт, треба кип`ятити протягом 5-ти годин на повільному вогні. При цьому в міру випару в розчин доливають дистильовану воду. Після цього в електроліт доливають воду й доводять об`єм до 1-го літра. Потім відстоюють протягом однієї години
Електроліт отфильтровивают через фільтрувальний папір для видалення гідрату окиси заліза, що осів на дно посудини